发布日期:2026-03-13 发布人:瑞科盟 点击量:214
在禽类养殖中,由大肠杆菌、沙门氏菌等引起的细菌性疾病,尤其是那些形成生物被膜的顽固性感染,正严重威胁着禽群健康与生产效益。面对细菌耐药性和生物被膜的双重堡垒,“噬菌体-抗生素组合”?疗法被视为一种极具潜力的绿色替代或协同治疗方案。
在禽类养殖中,由大肠杆菌、沙门氏菌等引起的细菌性疾病,尤其是那些形成生物被膜的顽固性感染,正严重威胁着禽群健康与生产效益。面对细菌耐药性和生物被膜的双重堡垒,“噬菌体-抗生素组合”?疗法被视为一种极具潜力的绿色替代或协同治疗方案。
然而,如何从海量的噬菌体与抗生素中,快速、准确地筛选出真正有效的“黄金搭档”,而非相互掣肘的“错误组合”,是推进该疗法在畜禽领域应用的核心瓶颈。在生物被膜模型上进行筛选不仅耗时费力。
近日,一项发表于国际期刊《Frontiers in Microbiology》上的研究,为这一难题提供了一个革命性的简化思路。这项虽以人医病原(金黄色葡萄球菌)为模型的研究,其方法论和核心结论,对禽用噬菌体制剂的研发与联合用药方案设计,具有极其重要的启示意义。
一、核心研究:用“简单”预测“复杂”
研究团队:荷兰莱顿大学医学中心
研究思路:能否用操作简便、周期短的游离细菌(planktonic bacteria)体外药敏试验结果,来预测治疗生物被膜(biofilm)感染时,噬菌体与抗生素组合的真实效果(协同、相加、拮抗)
实验设计精要:
模型选择:以临床分离的甲氧西林敏感金黄色葡萄球菌(MSSA)及其对应的烈性噬菌体ISP为模型。
抗生素组合:选取了6类作用机制不同的临床常用抗生素:靶向转录的利福平、环丙沙星;靶向蛋白合成的庆大霉素、克林霉素;靶向细胞壁的氟氯西林;靶向细胞膜的达托霉素。
双线验证:
游离菌:测试不同浓度抗生素与不同滴度噬菌体ISP组合,对游离态MSSA的杀灭效果及对噬菌体复制的影响。
生物被膜:在医用钛合金植入物模拟物上培养7天成熟生物被膜,模拟“植入物感染”场景,然后给予PAC连续1-3天的处理,评估杀菌效果。
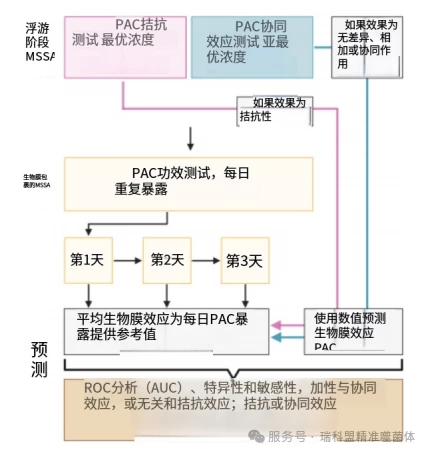
图1 用于预测噬菌体-抗生素组合(PAC)对包裹在生物膜中的甲氧西林敏感金黄色葡萄球菌(MSSA)有效性的实验装置概述。此处将加和效应与协同作用相结合,以表明有利效果;而将无影响和对抗作用归类为表明无助益效果。游离态和生物膜态PAC试验均基于细菌计数(菌落形成单位(CFU)/mL)的微生物计数结果,比较在接触PAC时的计数情况与单独使用各单一药物时的计数情况。此外,浮游生物拮抗试验评估了细菌接触PAC后噬菌体滴度(噬菌斑形成单位(PFU)/mL)与单纯接触噬菌体时的差异。图表由Biorender.com生成。
二、关键结果:惊人的“不对称”预测力
研究结果没有给出“简单完全等于复杂”的理想答案,但却指出了一个极具实践价值的“安全筛选路径”。
“排雷”能力卓越:游离菌试验能精准预测拮抗作用
数据说话:研究发现,在游离菌试验中,噬菌体ISP与利福平或庆大霉素的组合表现出明显的拮抗效应——抗生素的存在显著抑制了噬菌体的杀菌活性及其自身复制。
生物被膜验证:至关重要的是,这两种“坏组合”在真实的生物被膜感染模型中也同样失败,无法有效清除被膜内细菌。
预测效能:通过统计学分析(ROC曲线),游离菌试验对生物被膜拮抗作用的预测准确率(AUC > 0.89)。这意味着,如果在游离阶段看到“拮抗”,这个组合几乎可以确定在复杂的生物被膜感染中也无效,应直接淘汰。
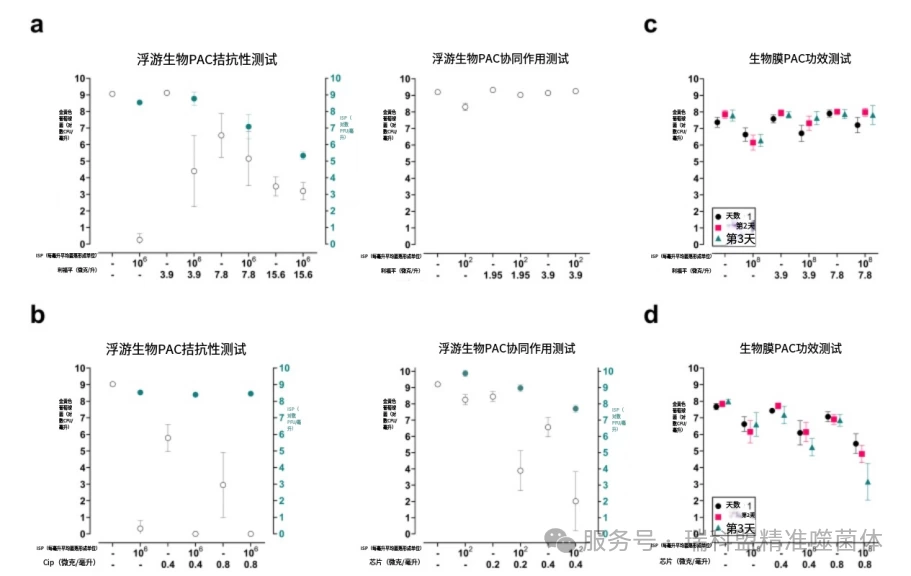
图2 噬菌体(噬菌体)ISP、靶向细菌转录的抗生素及其组合对浮游生物和生物膜包裹的甲氧西林敏感金黄色葡萄球菌(MSSA)。通过将MSSA暴露于中对数相106 CFU/mL,结合噬菌体ISP于106 PFU/mL(感染倍数(MOD) =1I)或ISP于102PFU/mL(MOl=0.0001)及以下次优浓度的MSSA暴露于PAC中,测试了其疗效。经过24小时的暴露(转速90rpm,温度37C)后,细菌通过离心(1,000xg,10分钟)被分离出来。随后,使用双琼脂覆盖法测定上清液中的噬菌体滴度(PFU/mL),并通过微生物学方法评估沉淀物中的细菌负载。在重新悬浮于含有10 mM铰硫酸盐()六水合物(FAS;用于中和残余噬菌体活性)的0.9%生理盐水中后,a和b中的开放(白色)符号表示平均CFU/mL,而封闭(蓝色)符号则表示平均PFU/mL。此外,PAC的功效在MSSA身上被评估,对象是在钛-6%铝-7%铌(Ti-6A-7Nb)植入体模型上形成的7天成熟生物膜。简言之,生物膜每日被暴露于ISP中,其浓度为10PFU/mL,同时与(c)利福平或(d)环丙沙星联合使用,持续多三天。每次暴露前后,均通过用0.9%生理盐水进行两次清洗来去除游离细菌。最后,通过超声处理(40kKHz,10分钟)在0.9%生理盐水中加入10 mMFAS来从生物膜中提取细菌,以进行微生物定量分析以测定细菌数量。脑-心灌注肉汤被用作所有试验中的稀释剂。所得结果来自至少三次独立实验,每项实验均进行三次重复。数据经对数转换处理,误差条表示95%的置信区间。
2. “寻优”能力有限:游离菌试验难以完全预测协同作用
复杂情况:相反,一些在游离菌试验中显示出协同潜力的组合(如ISP+环丙沙星/克林霉素/氟氯西林),虽然最终在生物被膜上也有效,但往往需要更高浓度、更长时间(2-3次暴露)的处理才能达到理想效果。
预测短板:游离菌试验模型低估了生物被膜的耐受性,无法预测出协同方案所需的剂量和疗程。单纯依靠游离菌试验的“协同”信号,可能会错过一些需要调整策略才有效的组合,或者对起效条件过于乐观。
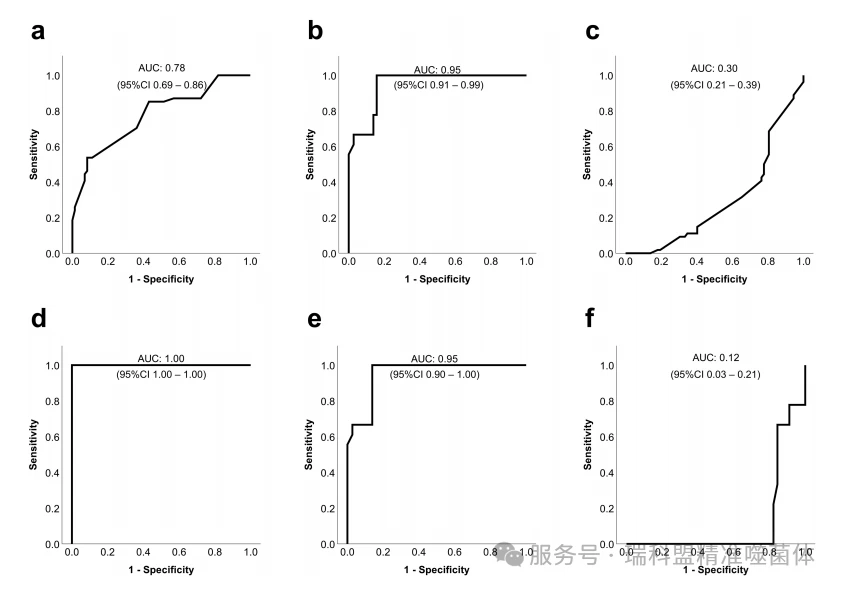
图3 检测噬菌体-抗生素组合物(PAC)对游离甲氧西林敏感金黄色葡萄球菌(MSSA)的性能,以预测PAC在每日三次接触后对包裹生物膜的MSSA的疗效。受试者工作特性(ROC)曲线被用来计算PAC对游离相MSSA的影响是否与PAC对生物膜包埋MSSA的影响相媲美。图表显示了在游离细菌预测的生物膜包裹MSSA上三次暴露后,抗生素与噬菌体ISP之间不利(无效、拮抗)效应(a,d)、拮抗效应(b,e)以及协同效应(G,f)。图a、b和c展示了所有经测试的PAC浓度所具有的预测能力,而图d、e和f则基于低抗生素浓度下PAC的值,这些值是在游离状态和生物膜包裹的 MSSA上进行测试得出的。AUC=曲线下面积。数据来自三次实验的三份重复样本,其中图a、b和c中每组PAC包含两到三个抗生素浓度,而图d、e及f中每组PAC包含一到两个抗生素浓度。
三、对禽用噬菌体研发的核心启示
这项研究虽非直接针对禽病原,但其科学范式为我们提供了清晰的研发路线图:
1. 确立高效、低成本的“一级筛查”流程
在禽用噬菌体-抗生素组合研发初期,应立即引入游离细菌组合药敏试验作为强制性的首轮筛选。核心目标不是找到“解”,而是快速、大批量地排除“错误答案”(即拮抗组合)。这能极大节约后续在复杂生物被膜模型或动物感染模型上的宝贵资源和时间,遵循“首先,不造成伤害”的原则。
2. 重点关注与禽用抗生素的相互作用机制
研究表明,相互作用高度依赖于抗生素的作用机制。在禽业中,氨基糖苷类(如庆大霉素、新霉素)、氟喹诺酮类(如恩诺沙星)、四环素类、β-内酰胺类等是常用药物。研发时,必须针对这些特定类别的抗生素,与候选噬菌体进行系统的游离水平拮抗/协同筛查。尤其要注意可能抑制噬菌体复制的蛋白质合成抑制剂。
3. 理解并跨越“游离”与“被膜”的鸿沟
游离试验是优秀的“守门员”,但非最终的“裁判”。通过一级筛查的组合,必须进入更贴近养殖业实际的“生物被膜模型”进行二级验证(如模拟禽呼吸道黏液、坏死组织或设备表面的被膜)。此阶段需重点评估:
剂量调整:可能需要提高抗生素或噬菌体的局部有效浓度。
给药策略:研究提示多次暴露(如连续饮水给药数日)可能比单次冲击更有效。
配方优化:需考虑如何让噬菌体和抗生素更好地渗透到被膜内部。
4. 为“个性化”或“场景化”治疗方案奠定基础
不同养殖场病原菌的耐药谱和流行株不同。未来,可以建立基于游离快速筛查的“噬菌体-抗生素配伍数据库”。当某养殖场出现疑似生物被膜相关顽固感染时,可分离病原菌,利用游离菌法快速测试其与现有噬菌体库及许可抗生素的配伍性,排除拮抗组合,初步圈定几个安全且有潜力的联合用药方案,再结合临床判断,实现快速、精准的干预。
总结
这项研究如同一盏明灯,照亮了噬菌体-抗生素联合疗法研发中一段最曲折的道路。它告诉我们:不要一开始就试图征服最复杂的堡垒,而是先用最简单的工具清扫掉明确的地雷。
对于禽用噬菌体领域而言,采纳这一“游离菌预筛,被膜验证”的研发策略,将能显著提升产品开发的效率和成功率,加速推出真正能解决养殖一线顽固性细菌感染问题的创新解决方案,为减抗、替抗战略提供更强大的技术武器。
论文原文索引:
Verheul M, et al. (2026) Efficacy prediction of bacteriophage-antibiotic combinations against Staphylococcus aureus biofilms using planktonic bacteria. Front. Microbiol. 16:1706083.
编译:盖春云
免责声明:本微信服务平台资料来源于网络收集,以供给大家学习、交流为目的,我们尊重资料原作者,支持正版。若所列资源侵犯了您的权益,请直接留言,我们将立刻删除!